Notice
Recent Posts
Recent Comments
Link
250x250
| 일 | 월 | 화 | 수 | 목 | 금 | 토 |
|---|---|---|---|---|---|---|
| 1 | 2 | 3 | ||||
| 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 |
| 18 | 19 | 20 | 21 | 22 | 23 | 24 |
| 25 | 26 | 27 | 28 | 29 | 30 | 31 |
Tags
- 날솟샘
- 웹개발
- SQL
- 설교
- 어노인팅
- FE
- SQLD
- 프론트엔드
- csee
- Database
- 화학
- dbms
- CHEMISTRY
- GLS
- 묵상
- 데이터베이스
- typeScript
- QT
- 일반화학
- 찬양
- 전산전자공학부
- 유태준교수님
- 혼자공부하는sql
- 예배
- 한동대학교
- 글로벌리더십학부
- CCM
- 남재창교수님
- 날마다 솟는 샘물
- Software Engineering
Archives
- Today
- Total
멈추지 않는 기록
[일반 화학] Chapter 2 - (2) 본문
728x90
2.3 Atomic Number, Mass Number, and Istopes (원자 번호, 질량 수, 동위원소)
[1] Atomic Number, Mass Number, and Istopes
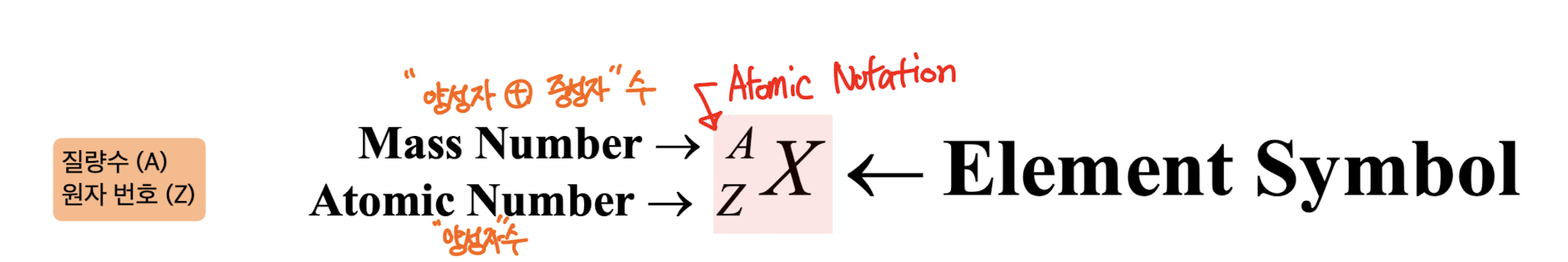
1) Atomic number (Z) : 핵의 양성자 수
- 원자 번호와 동일하다
- 고정적이다.
2) Mass Number (A) : 양성자 수(or 원자번호) + 중성자 수
- 고정적이지 않다.
중성자: 원자핵을 구성하는 것 중 전하3) Isotopes : 핵의 중성자 수가 다른 동일한 원소(X)의 원자
- 동일한 원소라도 중성자의 수에 따라 여러 가지 동위원소가 존재할 수 있습니다.
[2] The Isotopes of Hydrogen (수소의 동위원소)
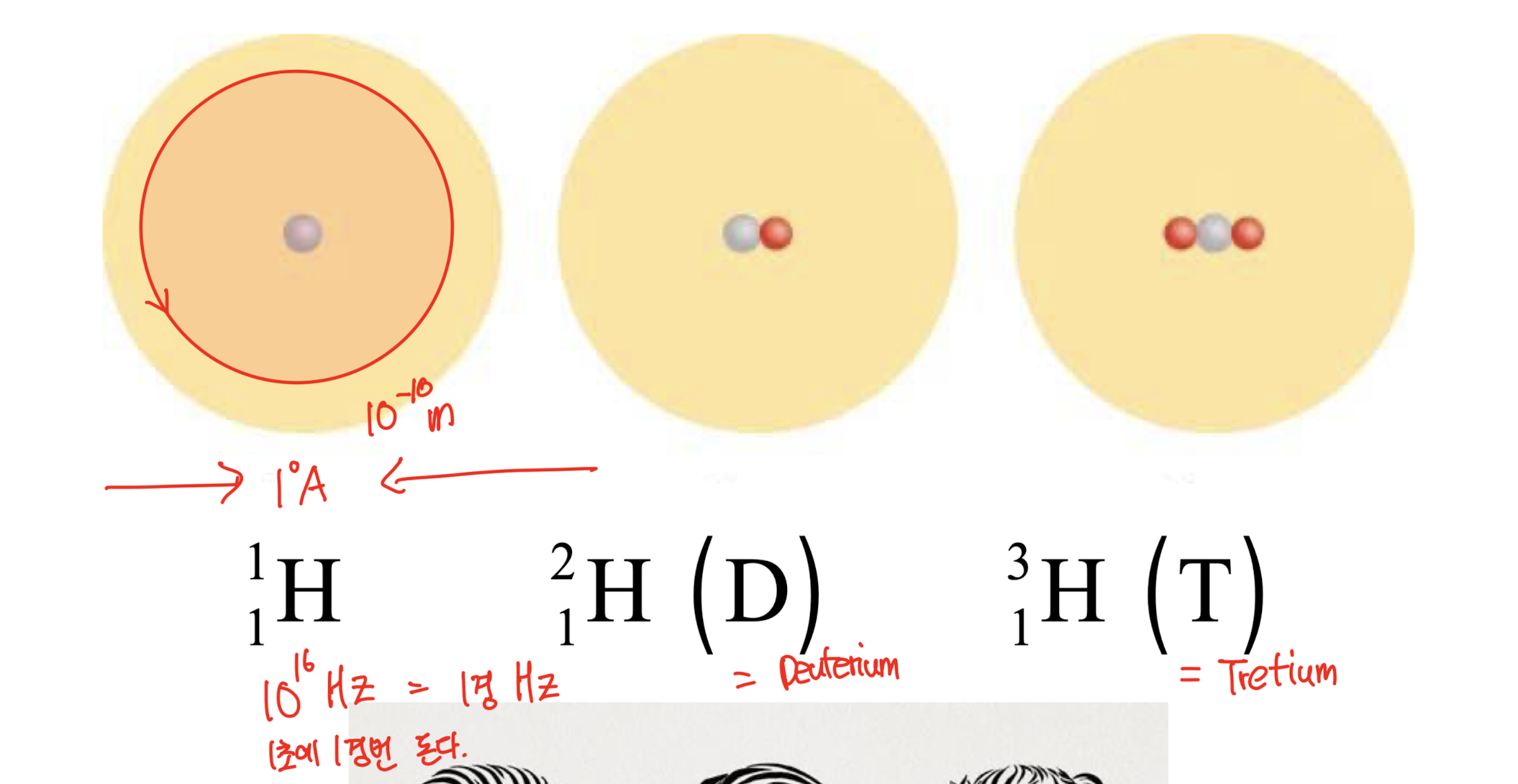
동일한 원소이지만, 핵의 중성자 수가 다르다.
2.4 The Periodic Table (주기율표)
[1] The Modern Perodic Table (현대 주기율표)
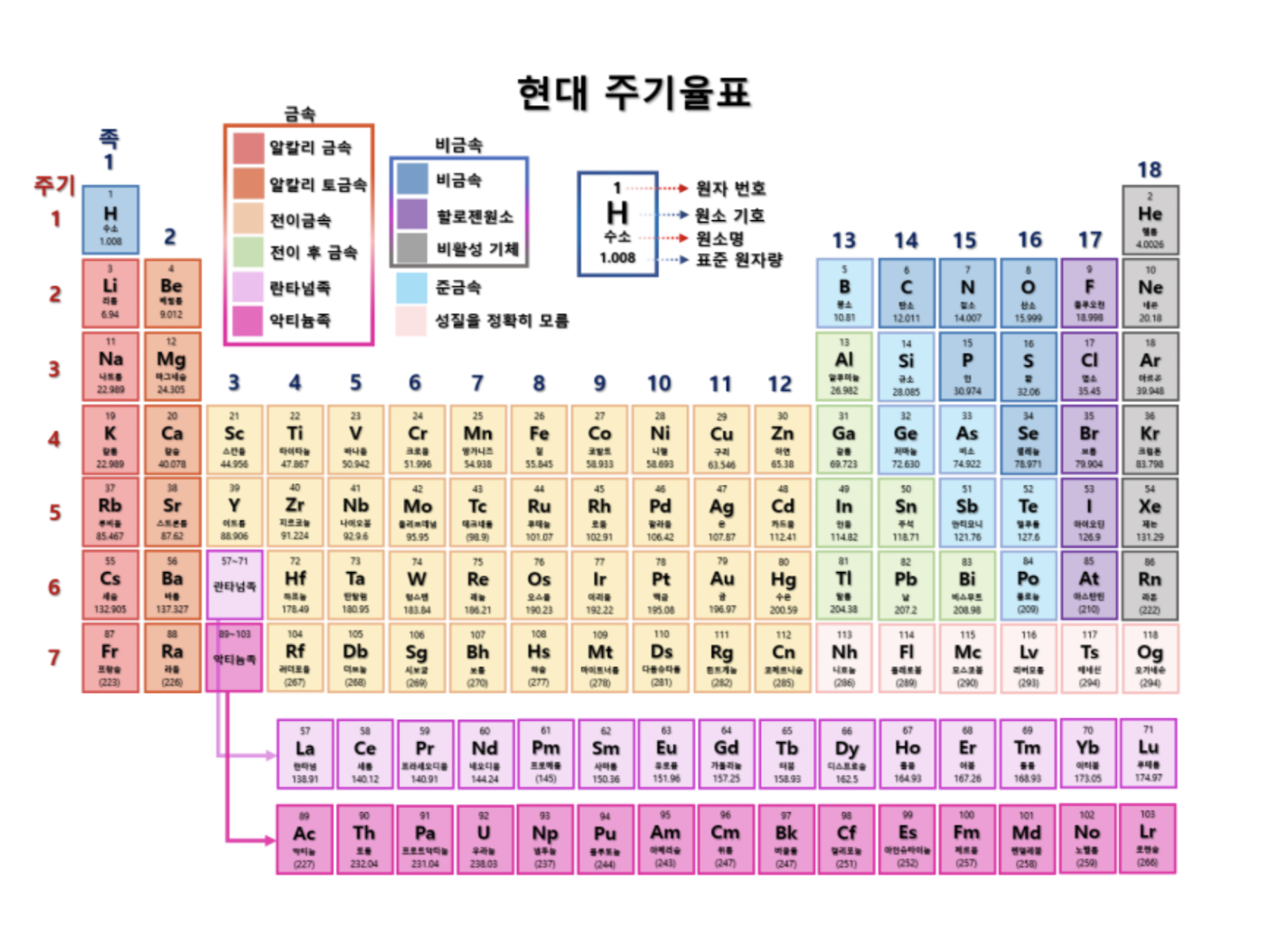
1) 특징
- 1열 : Alkali metal (알칼리 금속)
- 2열 : Alkaline metal (알칼리 토금속)
- 3열 우측부터 Metals : 전이금속
- 17열 : Halogan (할로젠 원소)
- 18열 : Noble (비활성 기체)
[2] Chemistry In Action (행동하는 화학)
1) 지구의 지각에 자연적으로 풍부한 원소들
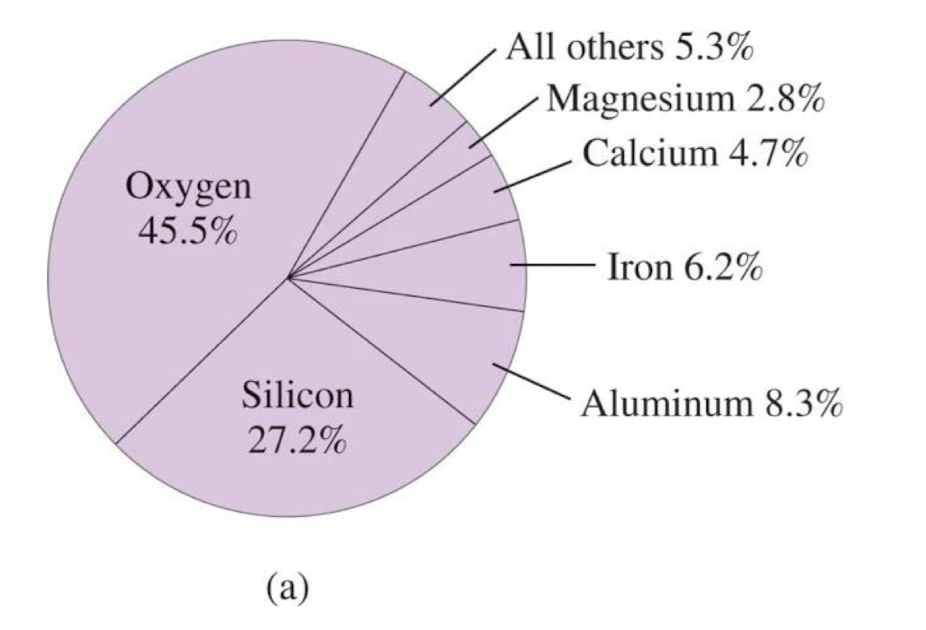
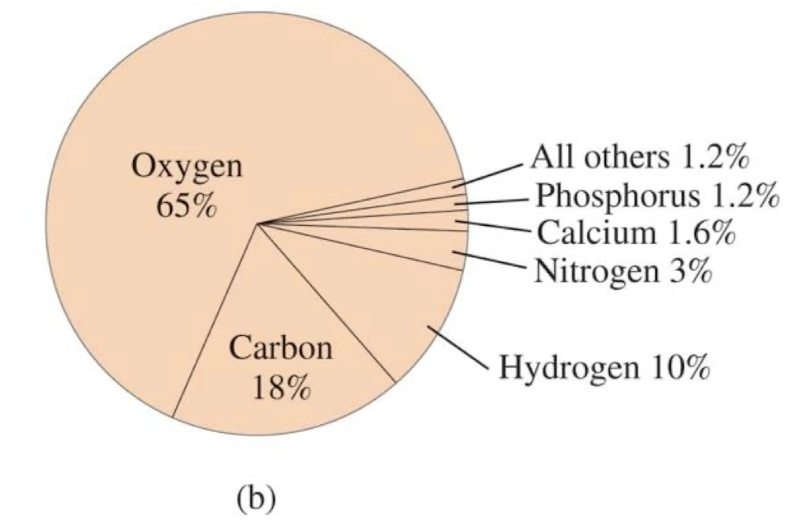
2) 인체에 자연적으로 풍부한 원소들
2.5 Molecules and Ions (분자와 이온)
[1] Molecules
: 두 개 이상의 원자가 화학적 힘에 의해 일정한 배열로 결합된 집합체
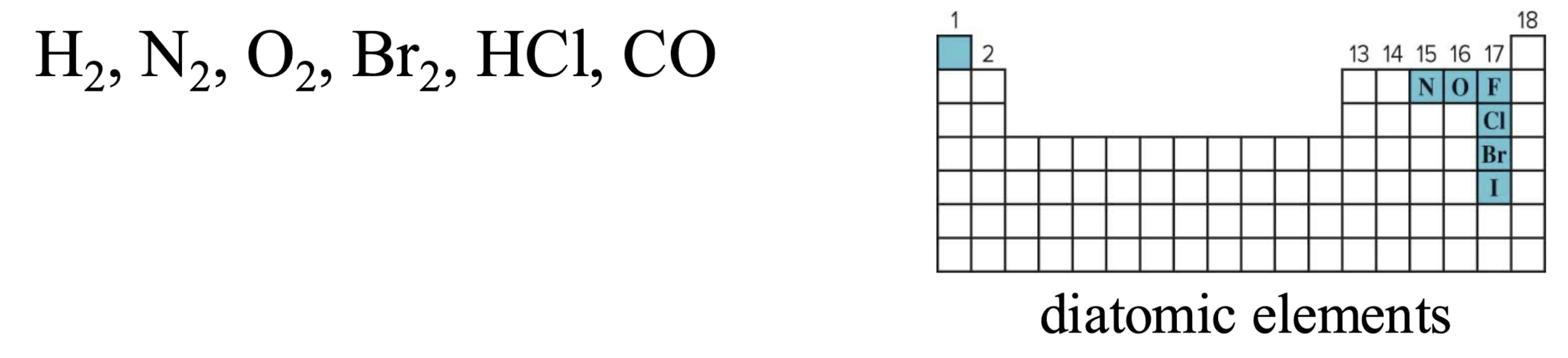
diatomic molecule (이원자 분자)
: 이원자 분자는 두 개의 원자만 포함한다.
: 같은 종류, 또는 다른 종류의 두 원자로 이뤄진 분자를 말한다.
- 동핵 분자 : 수소, 산소, 질소처럼 같은 종류의 원자로 이뤄진 경우
- 이핵 분자 : 일산화 탄소, 아이오딘화 칼륨, 염화 수소처럼 다른 종류의 원자로 이뤄진 경우
polyatomic molecule (다원자 분자)
: 다원자 분자는 두 개 이상의 원자를 포함한다. (2개 X, 3개 이상의 원자)
- 두 개의 원자로만 구성된 이원자 분자와 달리,
여러 원자가 결합하여 분자를 형성하는 경우
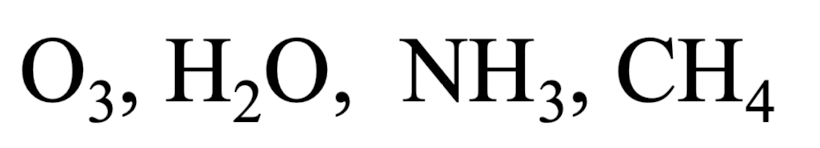
[2] Ions (이온)
: 양전하 또는 음전하를 띠는 원자 또는 원자 그룹
1) cation (양이온)
: 양전하를 띤 이온
- 중성 원자가 하나 이상의 전자를 잃으면 양이온이 된다. (전자를 하나 잃으면 양성자가 강해지니 +가 된다.)

2) anion (음이온)
: 음전하를 띤 이오
- 중성 원자가 하나 이상의 전자를 얻으면 음이온이 된다. (전자를 하나 얻으면 양성자가 약해지니 -가 된다.)

3) monatomic ion (단원자 이온)
: 원자를 하나만 포함하는 경우
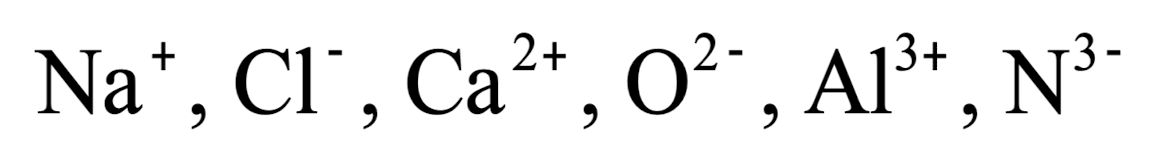
4) polyatomic ion (다원자 이온)
: 두 개 이상의 원자를 포함하는 경우
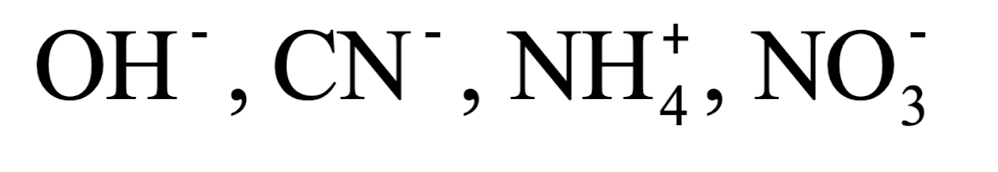
5) 흔한 이온
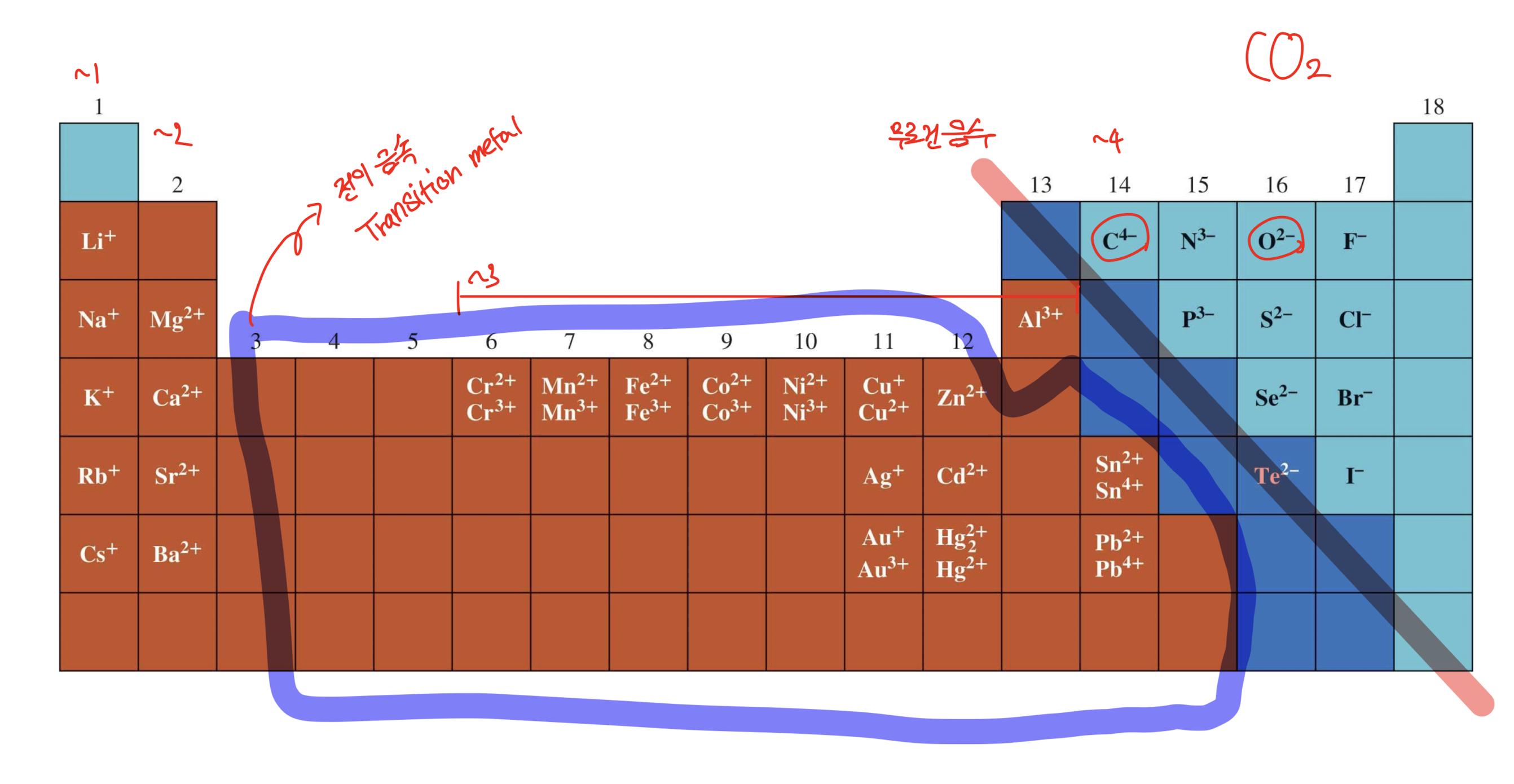
- 빨간색 부분은 '양이온을 나타내고, 파란색 부분은 '음이온'을 나타낸다.
- 원소가 전자를 잃거나 얻었을 대 만들어지는 흔한 이온 형태를 나타낸다.
- 전이 금속
- 3행 이후 14행까지의 Metal 부분 (명확하지 않으므로 추후 업데이트하자)
2.6 Chemical Formulas (화학 공식)
[1] Formulas and Models (공식과 모델)
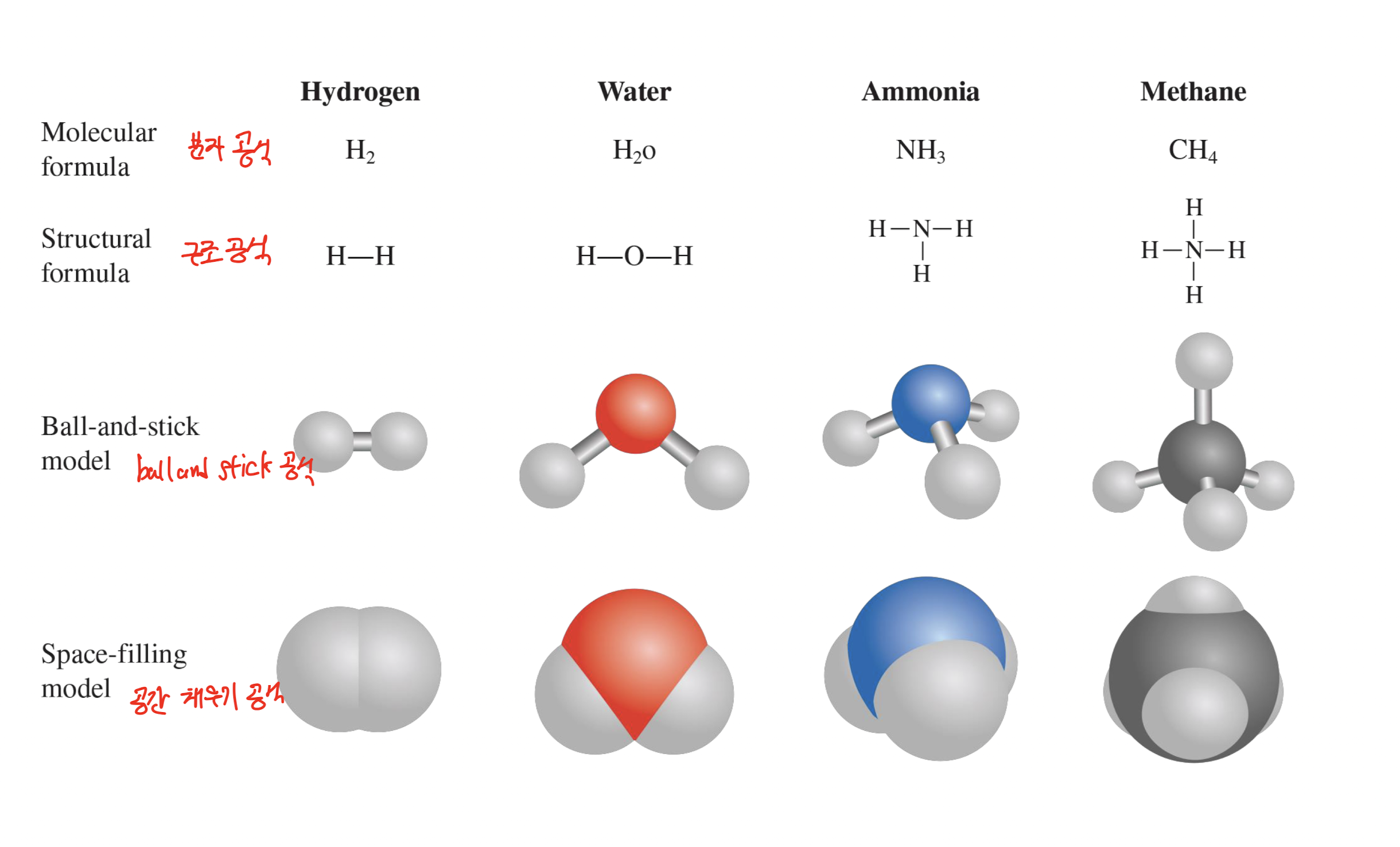
[2] Types of Formulas (수식 유형)
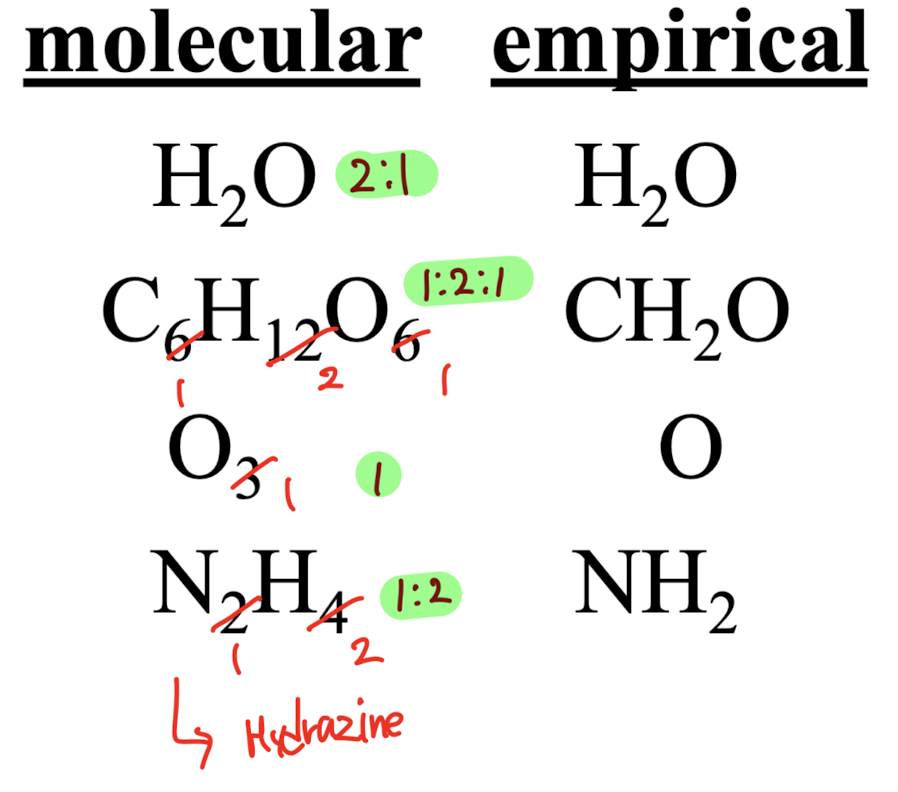
1) molecular formular (분자식)
: 분자식은 물질의 가장 작은 단위인 각 원소의 정확한 원자 수를 나타낸다..
2) empirical formula (실험식)
: 실험식은 물질에 포함된 원자의 가장 단순한 정수 비율을 나타낸다.
[3] Ionic Compounds (이온 화합물)
: 양이온과 음이온의 조합으로 구성된다.
1) 특징
- 일반적으로 경험식 공식과 동일하다.
- 이온 화합물은 결정 구조를 가지고 있기 때문에, 경험식 공식과 화학식이 동일하다.
- 각 화학식 단위에서 양이온과 음이온의 전하의 합은 0이어야 한다.
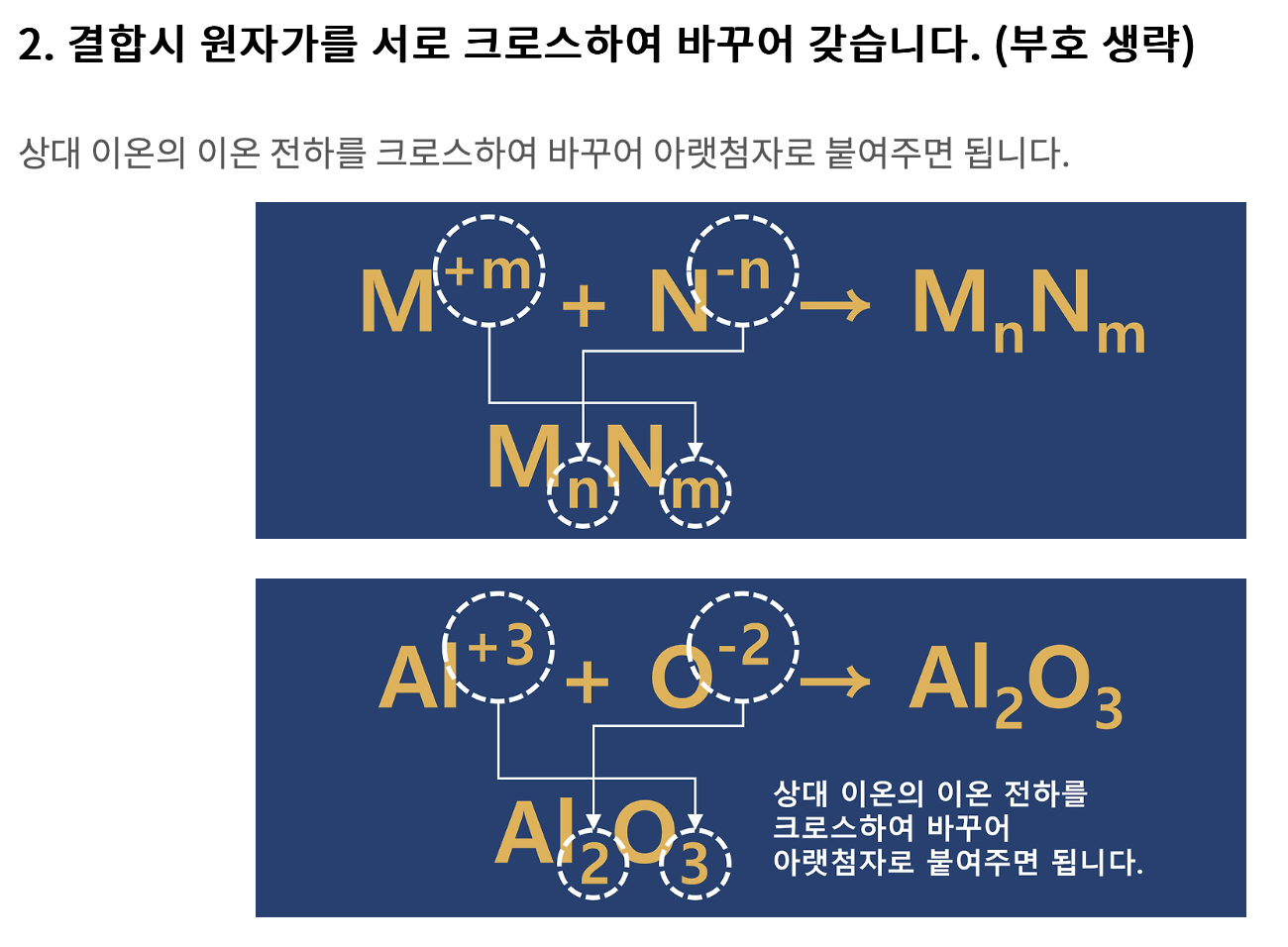
2) 표현 방법
2.7 Naming Compounds (명명법)
[1] Reactive Elements (반응형 요소)
: 화학적으로 활발히 반응하는 원소
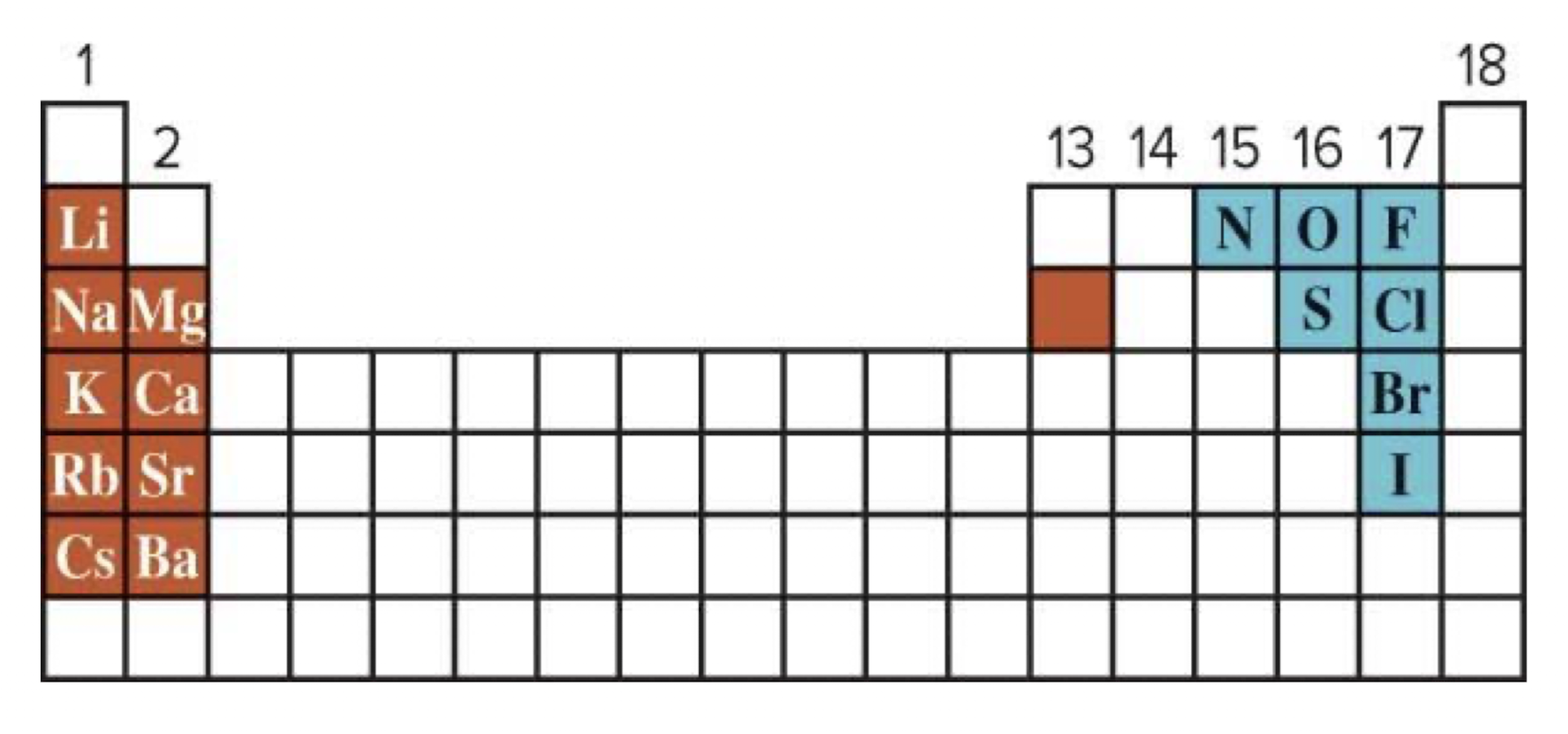
- 반응성이 가장 높은 금속(갈색)과 반응성이 가장 낮은 비금속(파란색)이 결합하여 이온 화합물을 형성한다.
[2] Formulas of Ionic COmpounds (이온 화합물의 공식)
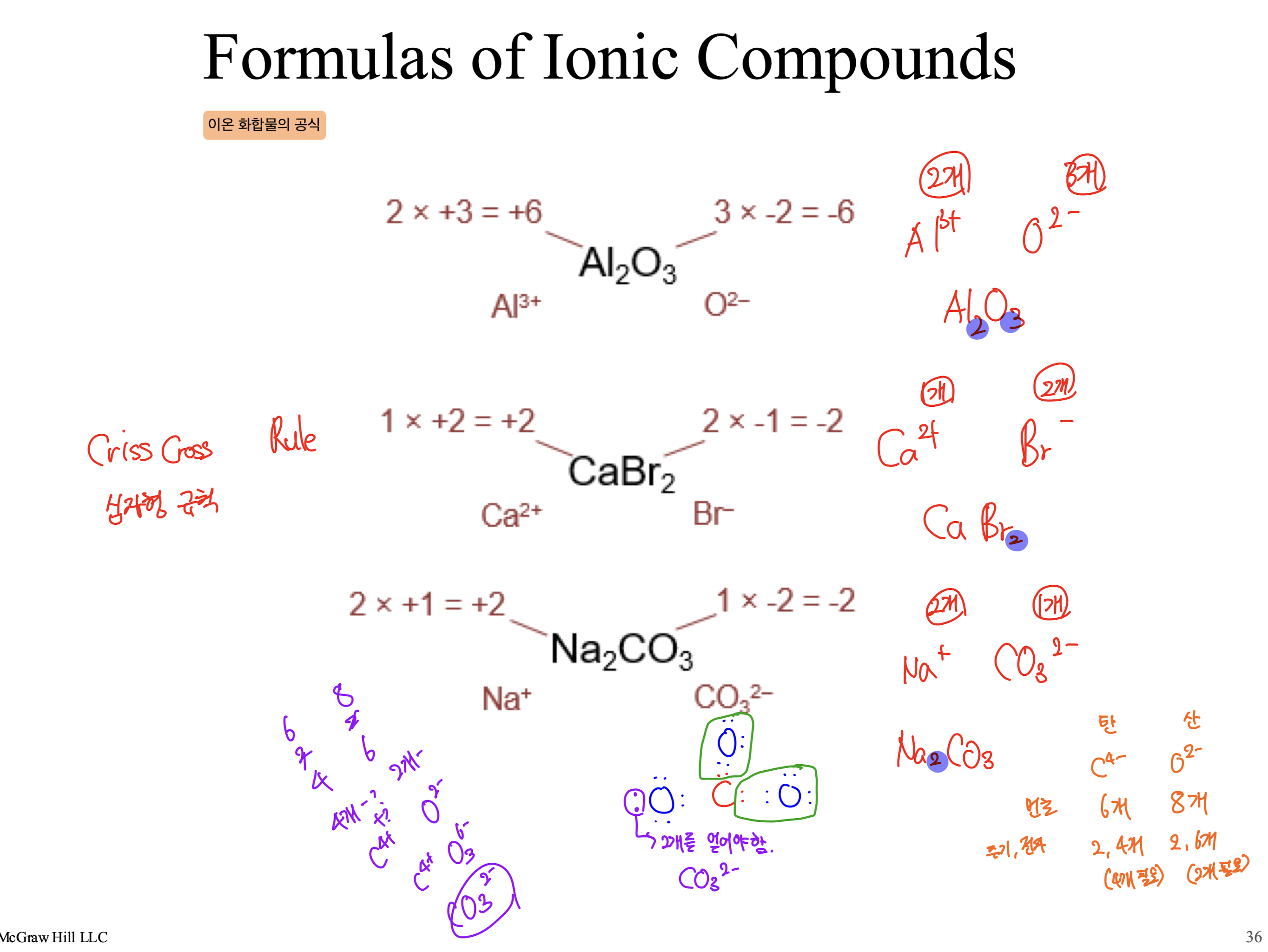
공식
1) 이온의 전하를 확인
2) 전하가 서로 상쇄되도록 이온의 개수를 조절
3) 화학식에 적절히 반영
그림으로 보는 방식

[3] Chemical Nomenclature (화학 명명법)
1) Ionic Compounds
- 금속 + 비금속
- 음이온(비금속) 원소 이름에 'ide' 추가

[4] Naming Transition Metal Ionic COmpounds (전이 금속 이온 화합물 이름 짓기)
1) 전이금속
: 3족에서 12족에 속하는 원소들로, 이들은 특유의 물리적, 화학적 성질을 가지고 있다.
- 다양한 상화 상태를 가질 수 있다. (ex. Fe2+ / Fe3+)
2) 주요 전이 금속
- 철(Fe): 산업적으로 매우 중요하며, 스틸을 만드는 데 사용됩니다.
- 구리(Cu): 전기 전도성이 뛰어나며 전선과 전자 기기에 사용됩니다.
- 금(Au): 주로 장신구와 전자 기기에 사용됩니다.
- 은(Ag): 장신구와 사진 촬영에 사용되며 뛰어난 전기 전도성을 가지고 있습니다.
3) Transition metal ionic compounds (전이 금속 이온 화합물)
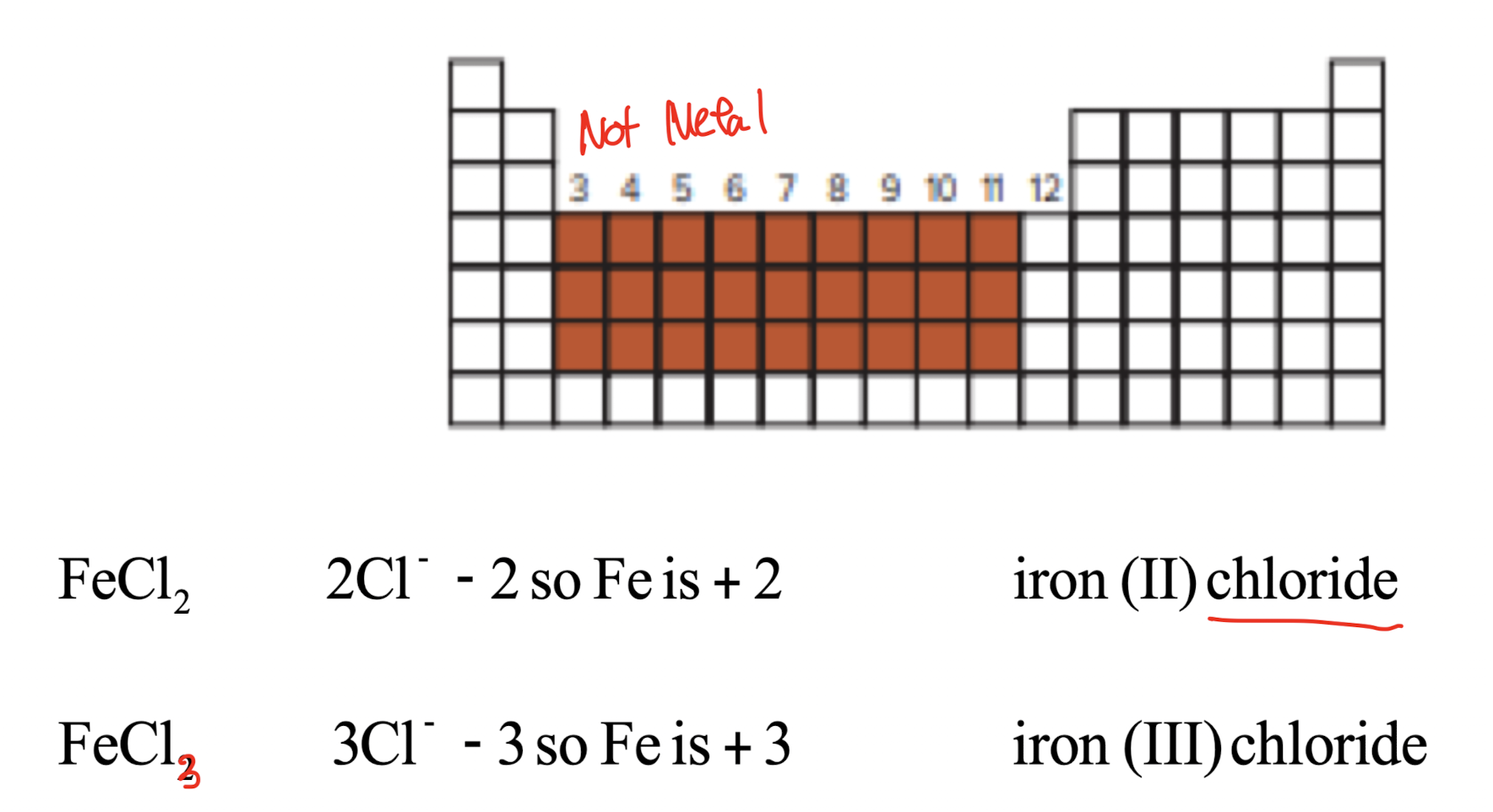
- 로마 숫자로 금속의 전하를 표시한다.
- ex) FeCl₂ = iron(II) chloride
: FeCl₂에서 "iron(2)"는 철이+2의 산화 상태를 가지고 있다는 의미
: 철은 다양한 산화 상태를 가질 수 있는데, 이 경우에는 철이 두 개의 염소 원자와 결합하면서 두 개의 전자를 잃어 +2의 산화 상태를 형성
: 반면 FeCl₃는 철(III) 클로라이드라고 불러서 철이 +3의 산화 상태를 가지는 걸 의미
[5] Naming Monatomic Anions (단원자 음이온 명명법)

- 'ide'를 붙인다.
[6] Common Inorganic Ions (일반적인 무기 이온)
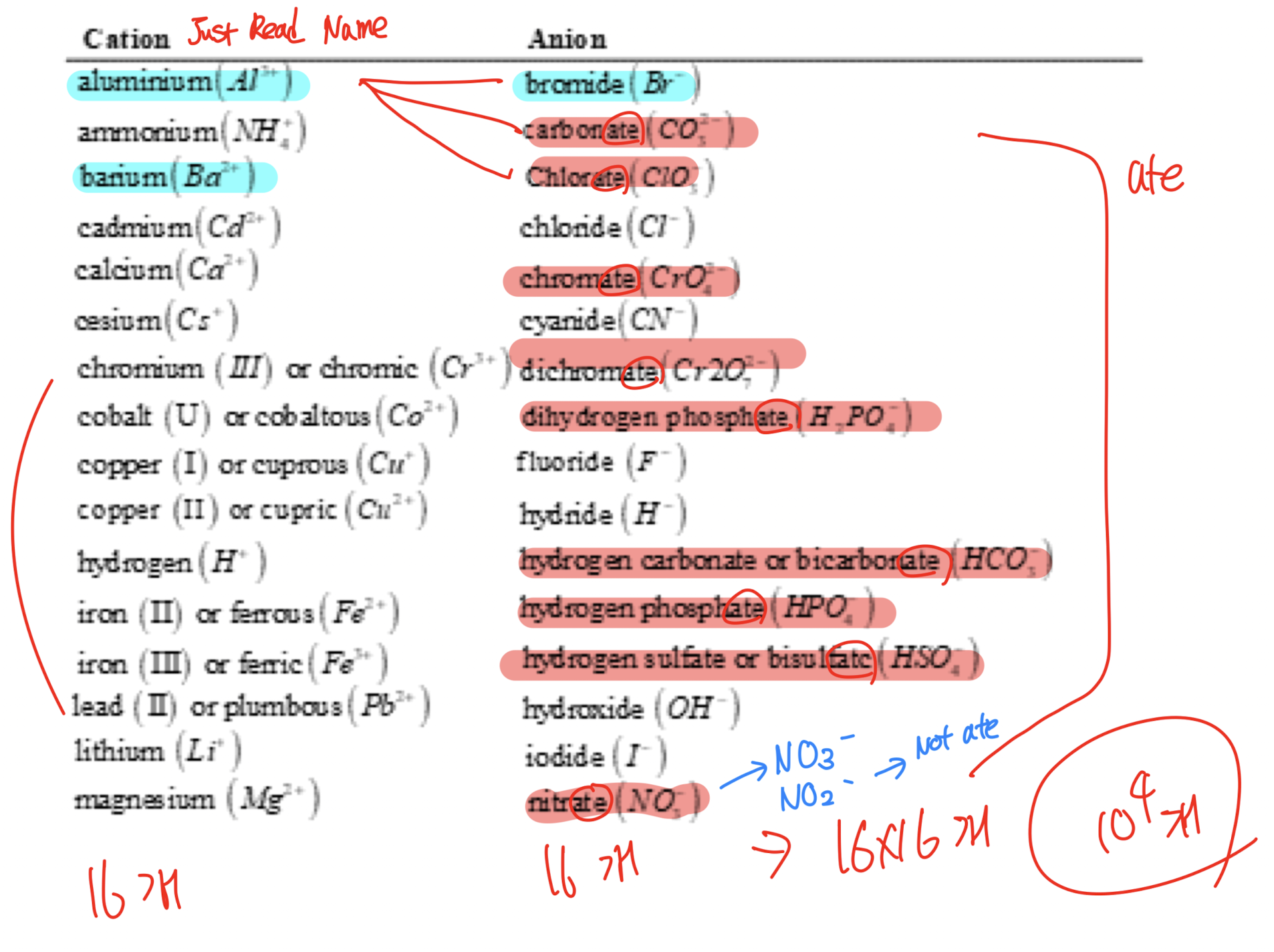
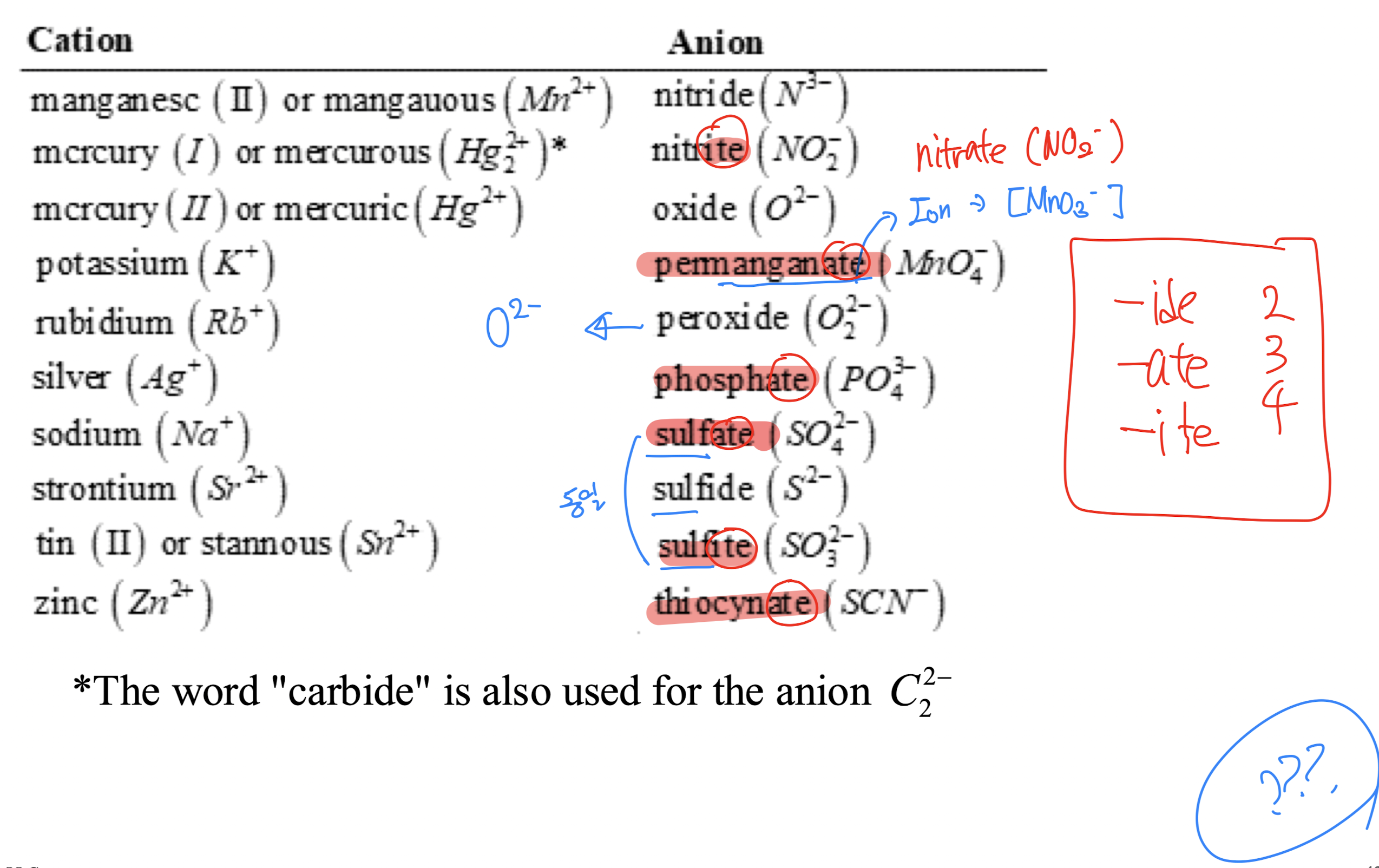
1) 물질 이름에서 -ide, -ate, -ite는 다음과 같은 의미를 가진다.
(1) -ide: 기본 음이온 이름에 붙어. 예를 들어:
- ex) Cl⁻: Chloride (염소가 음이온이 된 것)
(2) -ate: 산소를 포함한 음이온에 붙어. 보통 산화 상태가 높은 경우. 예를 들어:
- ex) SO₄²⁻: Sulfate (황이 산소와 결합한 것)
(3) -ite: -ate 이온에서 산소가 하나 적은 음이온에 붙어. 예를 들어:
- ex) SO₃²⁻: Sulfite (황이 산소와 결합했지만 -ate보다 산소가 하나 적은 것)
=> 즉, -ide는 기본 음이온, -ate는 산소가 많은 음이온, -ite는 산소가 적은 음이온을 나타내.

728x90
'한동대학교 > 일반화학' 카테고리의 다른 글
| [일반 화학] Chapter 3 -(1) (0) | 2025.03.14 |
|---|---|
| [일반 화학] Chapter 2 - (3) (0) | 2025.03.14 |
| [일반화학] Chapter 2 - (1) (0) | 2025.03.14 |
| [일반화학] Chapter 1 - (2) (0) | 2025.03.14 |
| [일반화학] Chapter 1 - (1) (0) | 2025.03.14 |




